Hyebin Yoo, Taisuke Nakahama, Reiichi Sugihara, Yu Gao, Yuta Ishizawa, Jingqi Yang, Zihan Ni, Miyu Iwasaki, Yuki Kato and Yukio Kawahara.Aberrant Multicellular Interferon Signaling Underlies Adar1 Mutation-Driven Aicardi-Goutières Syndrome-like Encephalopathy. Cell Rep. 2026 Apr 28: 45(4) 117113. doi: 10.1016/j.celrep.2026.117113.
https://www.cell.com/cell-reports/fulltext/S2211-1247(26)00191-9
研究成果の概要
ヒトを含めた哺乳類には、ウイルスなどに由来する外来性の撹乱RNAを認識するセンサー分子が発現しています。ウイルスなど異物が体内に侵入すると、この撹乱RNAを感知して自然免疫が活性化します。その結果、1型インターフェロン (IFN)が分泌され、ウイルスを排除するように作用します。こういった外来性撹乱RNAセンサー分子は、目印の付加された自己の内因性RNAには反応しません。しかし、内因性RNAへの目印付加などの機構に異常が生じると、センサー分子が内因性RNAを撹乱RNAと誤認し、自然免疫が異常活性化します。
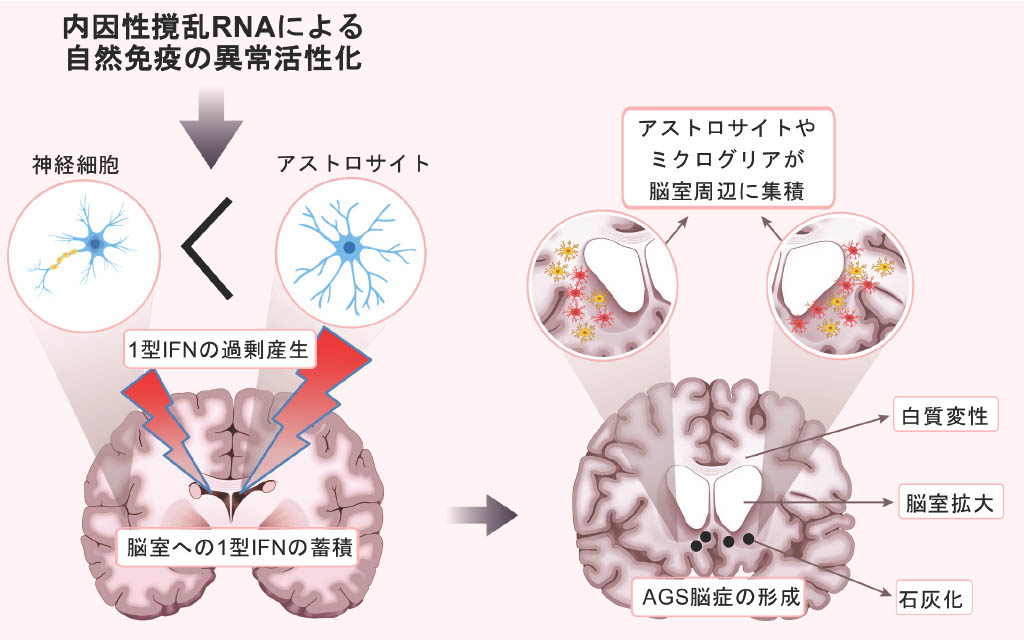
エカルディー・グティエール症候群 (AGS)は、先天的な自己炎症疾患で、自己核酸への目印付加や分解処理が正常に作動しないため、自然免疫が異常活性化し、1型IFNが過剰産生されています。AGSは脳症を主症状とし、脳室拡大、脳室周辺の石灰化、白質変性など、脳室周辺に強く症状が出現します。しかし、これまでAGS脳症が形成されるメカニズムは不明でした。RNA編集酵素をコードするADAR1は、AGS原因遺伝子の1つですが、河原らはマウスのAdar1遺伝子に左巻き2本鎖RNAへの結合が完全にできなくなる変異を挿入したところ、AGS脳症をよく再現するマウスを樹立することに成功しました (Nakahama et al, Immunity, 2021)。今回、このモデルマウスを活用することで、脳症形成に1型IFNが必要不可欠であること、脳内で直接1型IFNが過剰産生されており、特にアストロサイトの役割が大きいこと、1型IFNが脳室に蓄積し、脳室周辺で細胞の変性・脱落など病理学的変化が特に強いことを見出しました。これにより、長年不明であった内因性RNAが撹乱化した結果もたらされるAGS脳症の発症メカニズムを解き明かすことに成功しました。